Pour réguler cette activité métabolique, les systèmes tampon présents dans les milieux extracellulaires, intracellulaires et dans le tissu osseux permettent d’atténuer les variations du pH. Ces systèmes tampons sont régis par l’équation d’Henderson-Hasselbach. Pour simplifier le maintien de l’équilibre acido-basique est assuré par trois mécanismes:
- Les systèmes tampons (régulation à court terme)
- La ventilation pulmonaire
- L’excrétion rénale des H+
La régulation acido-basique va donc consister à ajuster la concentration plasmatique en H+ de façon à maintenir le pH du sang artériel à une valeur proche de 7,4. Les molécules qui libèrent des H+ (protons) en solution sont des acides. Inversement, tout substance qui peut accepter un H+ est une base.
- Système tampon acide carbonique/bicarbonate H2CO3 / HCO3-: Système tampon majeur dans les LEC que dans le LIC. Est un système tampon ouvert, c’est-à-dire qu’il possède une sortie vers l’extérieur de l’un de ses composants: élimination du Co2 par voie respiratoire et élimination des H+ et HCO3- par voie rénale.
- Système tampon phosphates: les phosphates sont les anions majoritaires du LIC. Ils sont en revanche minoritaires da,s les LEC dont le plasma. Ce système tampon jour un rôle majeur dans la régulation du pH cytosolique (cytosol => raction fluide de la matrice cytoplasmique) mais aussi l’urine.
- Système tampon des protéines: les protéines contenues dans le plasma et les cellules constituent le système tampon le plus abondant et assurent les trois quarts du tamponnage des liquides corporels. L’hémoglobine est un tampon efficace dans les hématies, tandis que l’albumine est la principale protéine tampon du plasma. Les protéines sont constituées d’acides aminés dont les chaînes latérales (R) peuvent se comporter comme des acides ou des bases. Par conséquent une protéine peut jouer le rôle d’un acide ou d’une base suivant le pH du milieu dans lequel elle se trouve.
Les systèmes tampons ont cependant des limites: ils ne sont efficaces que dans une petite fourchette de pH. De plus il n’y a pas de changement global du bilan des H+. Un système tampon ne résout donc pas le problème à long terme. Le contrôle à long terme se fait donc par le biais de deux organes: les poumons et les reins qui ont une action sur l’efficacité du tampon ouvert H2CO3-/HCO3-.
- Lors d’une HYPERCAPNIE, le CO2 s’accumule dans le sang mais aussi dans le LCR. La concentration en H+ augmente, ce qui stimule les chémorécepteurs centraux bulbaires. S’en suit une augmentation de la ventilation qui favorise l’élimination du CO2.
- Lors d’une HYPOCAPNIE, l’augmentation du pH sanguin baisse l’activité du centre respiratoire. La ventilation diminue, les respirations deviennent superficielles et le CO2 s’accumule dans le sang. La concentration en H+ augmente, le pH diminue pour revenir à sa valeur normale.
- En cas d’acidose: les H+ formés dans la cellule tubulaire sont excrétés dans l’urine, les HCO3- réabsorbés vers le sang. Le pH de l’urine diminue.
- En cas d’alcalose: les HCO3- formés dans la cellule tubulaire sont excrétés dans l’urine, les H+ réabsorbés vers le sang. Le pH de l’urine augmente.
- Le CO2 est produit par combustion métabolique +++
- Acide phosphorique et sulfurique = métabolisme des protéines soufrées, phosphorées et phospho-amino-lipides (apport protéique alimentaire : viandes surtout) peut engendrer des pathologies comme la crise de goutte.
- BILAN = apports alimentaires + métabolisme conduisent à une surcharge d’acide nette
- Tampons intracellulaires se trouvent dans les hématies, autres cellules et vont stabiliser le pH intracellulaire (hémoglobine +++ / les protéines / le phosphate: ATP)
- Tampons extracellulaires se trouvent dans le plasma, LCR, autres et stabilisent le pH extracellulaire (le HCo3- ou Bicarbonate présent dans le plasma / NH3 ammoniaque)
- Dans les poumons: CO2 (expiré) + H2O <= => H2CO3 (via l’anhydrase carbonique)<= => H+ + HCO3- !!!! Attention action réversible ce qui explique pourquoi le CO2 dans les poumons doit être expiré
- Les REINS agissent en 24/48 heures et vont éliminer les ions H+ mais attention il ne faut pas que les urines soient trop acides pour ne pas détruire les protéines circulantes dans les tubes urinifères et la vessie. Sécrétion par les reins de NH3 => NH3 + H+ => NH4 (ammonium). Intervention du SNC pour la sécrétion d’aldostérone (qui va augmenter la sécrétion d’H+ dans les urines). Le HCO3- est en grande partie recyclé par les reins
- PaCO2 = CAPNIE
Toute hyperventilation compense des acidoses métaboliques -> baisse du PCO2 = vasoconstriction = hausse du pH (tête qui tourne) = alcalinisation = pour résoudre le problème on fait une apnée - Les compensations agissant sur PaCO2 sont ventilatoires et immédiates
- Les compensations agissant sur HCO3- sont rénales et d’installation lente
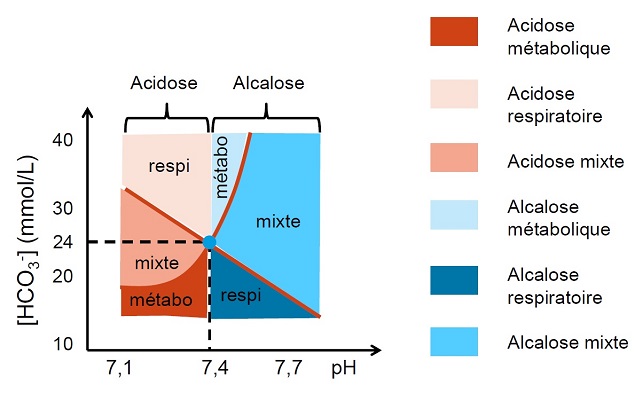
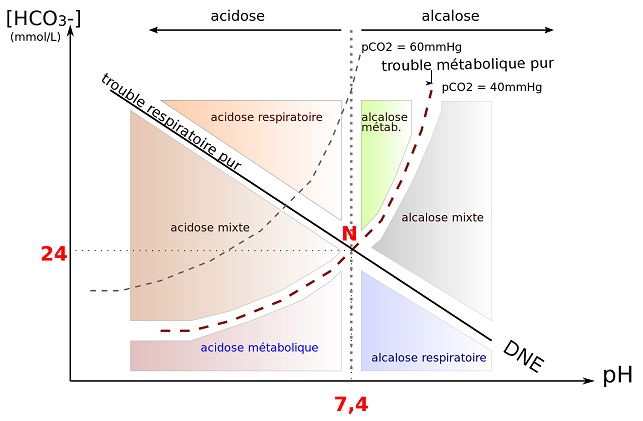
pH: 7.35 – 7.45
PaO2: 80 -105 mmHg
PaCO2: 35-45 mmHg
HCO3-: 21-28 mmol/l
CO2 total: 22-29 mmol/l
Causes possibles d’acidose respiratoire:
- Maladies qui diminuent la ventilation: coma, BPCO, myopathie
Causes possibles d’acidose métabolique:
- Maladies qui diminuent HCO3-: diarrhées, insuffisance rénale
- Maladies qui augmentent H+: acidocétose diabétique, baisse de tension importante
Causes possibles d’alcalose respiratoire:
- Augmentation de la ventilation: hypoxémie, troubles neurologiques, douleur
Causes possibles d’alcalose métabolique:
- Diurétique de l’Anse
- Fuite d’acides: vomissements